Biomolekul
Biomolekul adalah senyawa organik yang dapat ditemukan dalam tubuh makhluk hidup. Pada umumnya biomolekul adalah senyawa yang berukuran relatif besar, sehingga beberapa jenis biomolekul termasuk makromolekul. Dalam artikel ini akan dibahas empat kelompok biomolekul yang utama pada makhluk hidup, yaitu karbohidrat, protein, lipid, dan asam nukleat.
Karbohidrat
Nama karbohidrat (“hidrat karbon”) berasal dari rumus empiris senyawa-senyawa kelompok ini yang dapat dinyatakan dengan Cx(H2O)y. Sebagai contoh, glukosa memiliki rumus molekul C6H12O6 atau C6(H2O)6. Namun, karbohidrat sebenarnya bukanlah hidrat dari karbon. Karbohidrat merupakan senyawa polihidroksialdehida ataupun polihidroksiketon.
Kelarutan dan Hasil Kali Kelarutan (ksp)
Hukum Dasar Kimia: Lavoisier, Proust, Dalton, dll
Tabel Periodik Unsur Kimia
Penggolongan karbohidrat
Berdasarkan hasil hidrolisisnya, karbohidrat dapat dikelompokkan menjadi:
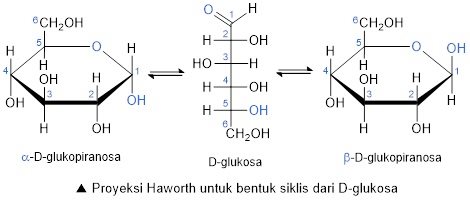
- Monosakarida, yaitu karbohidrat yang paling sederhana, tidak dapat dihidrolisis menjadi karbohidrat yang lebih sederhana. Misalnya, glukosa, fruktosa, ribosa, dan galaktosa.

- Disakarida, yaitu karbohidrat yang bila dihidrolisis terurai menjadi dua molekul monosakarida. Misalnya:
-
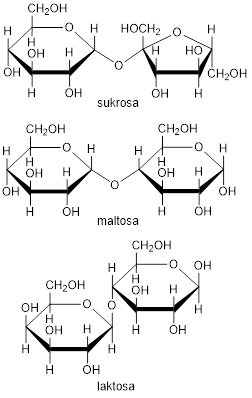
- sukrosa terdiri dari satu molekul glukosa dan satu molekul fruktosa
- maltosa terdiri dari dua molekul glukosa
- laktosa terdiri dari satu molekul glukosa dan satu molekul galaktosa
- Polisakarida, yaitu karbohidrat yang bila dihidrolisis terurai menjadi banyak (lebih dari 10) molekul monosakarida. Misalnya:
-
- amilum (pati) yang merupakan polimer dari D-glukosa.
Amilum dapat dipisahkan menjadi dua bagian, yaitu amilosa (~20%) dan amilopektin (~80%). Amilosa berbentuk rantai lurus dengan ikatan glikosida α-1,4’-. Amilopektin berbentuk rantai bercabang yang juga dihubungkan ikatan α-1,4’, dengan percabangan melalui ikatan glikosida α-1,6’.
- amilum (pati) yang merupakan polimer dari D-glukosa.
-
- glikogen yang merupakan polimer dari D-glukosa bercabang dengan ikatan glikosida α-1,4’- dan α-1,6’-.
- selulosa yang merupakan polimer dari D-glukosa lurus dengan ikatan glikosida β-1,4’-.

Uji karbohidrat
- Uji Molisch
Uji ini digunakan untuk menunjukkan adanya karbohidrat dalam sampel. Mula-mula larutan sampel diberi beberapa tetes larutan α-naftol, lalu diberi H2SO4 pekat secukupnya hingga terbentuk dua lapisan cairan. Bila terbentuk cincin warna merah keunguan, larutan sampel mengandung karbohidrat.
- Uji Fehling dan Uji Benedict
Uji ini digunakan untuk menunjukkan adanya gula pereduksi, yaitu monosakarida dan disakarida (kecuali sukrosa). Gula pereduksi akan bereaksi dengan pereaksi Fehling ataupun pereaksi Benedict menghasilkan endapan merah bata Cu2O.
- Uji iodin
Uji ini digunakan untuk menunjukkan adanya amilum. Larutan sampel yang mengandung amilum (amilosa) setelah diberi larutan iodin akan menghasilkan warna biru.
Protein
Protein merupakan polimer dari asam α-amino. Massa molekul realtifnya berkisar dari 6000 hingga beberapa juta. Unsur utama penyusun protein adalah C, H, O, dan N.
Asam amino
Asam amino merupakan suatu golongan senyawa karbon yang setidaknya mengandung satu gugus karboksil (−COOH) dan satu gugus amino (−NH2). Asam amino dalam protein disebut juga asam α-amino, karena gugus aminonya terikat pada atom C-α (atom C yang terikat langsung pada gugus karboksil). Struktur umum dari asam amino ditunjukkan pada gambar berikut.

Asam amino yang satu dengan asam amino yang lain berbeda pada gugus −R yang terikat pada atom C-α. Berikut terdapat 20 macam asam amino yang umum dikenal.

Protein tersusun dari sekitar 20 macam asam amino tersebut yang dapat dibedakan menjadi asam amino esensial dan asam amino nonesensial. Asam amino esensial adalah asam amino yang tidak dapat disintesis di dalam tubuh manusia, sehingga harus disuplai dari makanan. Asam amino esensial terdiri dari 10 macam, yaitu histidin, arginin, valin, leusin, isoleusin, treonin, triptofan, lisin, metionin, dan fenilalanin. Asam amino nonesensial adalah asam amino yang dapat disintesis dalam tubuh manusia.
Sifat-sifat asam amino:
- dapat membentuk ion zwitter, yaitu ion dipolar yang terbentuk dari reaksi asam-basa intramolekul

- bersifat amfoter (dapat bereaksi dengan asam maupun dengan basa)
- merupakan senyawa optis aktif, kecuali glisin
- dapat berikatan dengan asam amino lain melalui ikatan peptida

Struktur protein
Struktur protein dapat dibedakan ke dalam empat tingkatan, yaitu:
- Struktur primer: urut-urutan asam amino dalam rantai polipeptida.
- Struktur sekunder: susunan rantai polipeptida menggulung seperti spiral (heliks-α) ataupun berbaris bersisian (lembar-β) oleh karena adanya gaya-gaya nonkovalen, seperti ikatan hidrogen.
- Struktur tersier: susunan tiga dimensi dari struktur sekunder yang terbentuk melalui ikatan hidrogen, ikatan disulfida, interaksi hidrofobik/hidrofilik, serta ikatan ion.
- Struktur kuartener: susunan tiga dimensi yang terdiri atas beberapa rantai peptida.
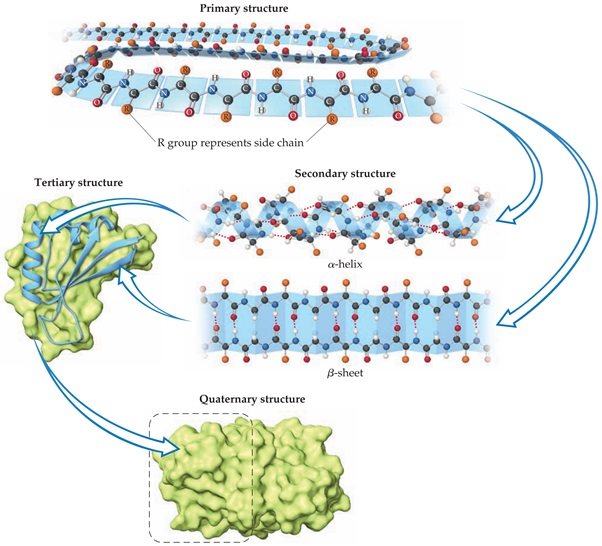
Struktur protein: primer, sekunder, tersier, dan kuarterner Sumber gambar: Brown, Theodore L. et al. 2015. Chemistry: The Central Science (13th edition). New Jersey: Pearson Education, Inc.
Uji protein
- Uji Ninhidrin
Uji ini digunakan untuk menunjukkan adanya asam amino dan/atau protein dalam sampel. Mula-mula larutan sampel diberi beberapa tetes larutan ninhidrin yang tidak berwarna, lalu dipanaskan beberapa menit. Bila terbentuk warna ungu, larutan sampel mengandung asam amino atau protein.
- Uji Biuret
Uji ini digunakan untuk menunjukkan adanya ikatan peptida, sehingga dapat mendeteksi protein namun tidak dapat mendeteksi asam amino bebas. Mula-mula larutan sampel ditetesi larutan NaOH, lalu ditetesi larutan CuSO4 encer. Jika terbentuk warna ungu, larutan sampel mengandung protein.
- Uji Xantoproteat
Uji ini digunakan untuk menunjukkan adanya protein yang mengandung gugus fenil (cincin benzena). Bila protein yang mengandung cincin benzena dipanaskan dengan asam nitrat pekat, maka akan terbentuk warna kuning yang dapat berubah menjadi jingga jika dibuat alkalin (basa) dengan larutan NaOH.
- Uji Belerang
Uji ini digunakan untuk menunjukkan adanya unsur belerang (sulfur) dalam protein. Mula-mula larutan protein yang telah ditetesi larutan NaOH pekat dipanaskan, lalu diberi beberapa tetes larutan timbal(II) asetat. Jika terbentuk endapan hitam (PbS), protein tersebut mengandung belerang.
Lipid
Lipid merupakan kelompok biomolekul yang terdiri dari beragam senyawa organik tidak larut dalam air, tetapi larut dalam pelarut-pelarut organik nonpolar seperti kloroform dan eter. Penggolongan lipid cenderung didasarkan pada sifat fisik (kelarutan), bukan pada struktur senyawa. Berikut akan dibahas tiga golongan lipid yang penting, yaitu:
Lemak dan minyak
Lemak (fat) seperti mentega dan minyak (oil) seperti minyak kelapa, merupakan ester dari gliserol dengan asam-asam lemak. Oleh karena itu, lemak dan minyak sering juga disebut sebagai trigliserida. Perbedaan utama dari lemak dan minyak adalah wujudnya dalam suhu ruang. Lemak mengandung lebih banyak asam lemak jenuh sehingga berwujud padat pada suhu ruang. Sedangkan, minyak mengandung lebih banyak asam lemak tak jenuh sehingga berwujud cair pada suhu ruang.
Berikut struktur umum dari trigliserida (lemak dan minyak), dengan R1, R2, dan R3 adalah rantai hidrokarbon yang jumlah atom karbonnya dari 3 hingga 23.

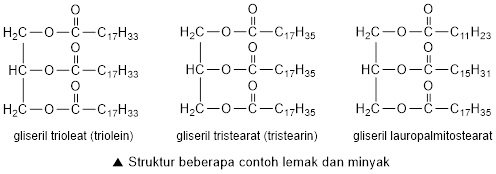
Lemak merupakan lipid yang dapat mengalami reaksi hidrolisis dengan menggunakan asam kuat atau enzim lipase. Hasil hidrolisis lemak adalah gliserol dan asam lemak.
Fosfolipid
Fosfolipid juga merupakan ester dari gliserol yang hanya terdapat dua asam lemak yang terikat pada gliserol sedangkan gugus alkohol yang ketiga mengikat gugus fosfat. Berbeda dengan lemak yang bersifat hidrofob, fosfolipid bersifat amfifilik, karena terdiri dari ekor nonpolar yang hidrofob dan kepala polar yang hidrofil.

Steroid
Steroid merupakan lipid tak terhidrolisis yang bukan golongan ester. Struktur dasar steroid terdiri dari 17 atom karbon yang membentuk sistem cincin tetrasiklik.

Asam Nukleat
Asam nukleat adalah biomolekul yang berperan penting dalam penurunan sifat-sifat genetik dan sintesis protein. Ada dua jenis asam nukleat, yaitu asam deoksiribonukleat (DNA = deoxyribonucleic acid) dan asam ribonukleat (RNA = ribonucleic acid). DNA maupun RNA merupakan polimer dari nukleotida. Nukleotida terdiri atas tiga komponen, yaitu:

- Gula pentosa
Gula pentosa penyusun DNA adalah 2-deoksi-D-ribosa, sedangkan gula pentosa penyusun RNA adalah D-ribosa.

- Gugus fosfat
Gugus fosfat menghubungkan satu nukleotida dengan nukleotida yang lain. Pada gugus fosfat terbentuk ikatan fosfodiester yang mengikat gula pentosa dari dua molekul nukeotida.
- Basa nitrogen
Lima basa nitrogen yang menyusun asam nukleat adalah adenin, guanin, sitosin, timin, dan urasil. Adenin, guanin, dan sitosin terdapat pada DNA maupun RNA. Sedangkan, timin hanya terdapat pada DNA dan urasil hanya terdapat pada RNA.

Contoh Soal Biomolekul dan Pembahasan
Contoh Soal 1
Pereaksi yang digunakan untuk mengidentifikasi gugus fungsional aldehida dalam glukosa adalah ….
A. pereaksi Biuret
B. pereaksi ninhidrin
C. kertas timbal asetat
D. pereaksi Fehling
E. larutan kanji
Jawaban: D
Glukosa termasuk gula pereduksi yang bereaksi positif dengan pereaksi Fehling menghasilkan endapan merah bata.
Contoh Soal 2
Berikut data hasil percobaan uji protein.
| Sampel | Tes | ||
| Biuret | Xantoproteat | Pb-asetat | |
| P | ungu | jingga | hitam |
| Q | ungu | − | − |
| R | ungu | − | hitam |
| S | ungu | jingga | − |
| T | ungu | − | − |
Berdasarkan data di atas maka protein yang mengandung gugus inti benzena adalah ….
A. P dan Q
B. P dan R
C. P dan S
D. Q dan S
E. Q dan T
Jawaban: C
Protein yang mengandung gugus inti benzena akan bereaksi positif dalam uji Xantoproteat menghasilkan warna jingga.
Referensi
Brown, Theodore L. et al. 2015. Chemistry: The Central Science (13th edition). New Jersey: Pearson Education, Inc.
Johari, J.M.C. & Rachmawati, M. 2008. Kimia SMA dan MA untuk Kelas XII Jilid 3. Jakarta: Esis
McMurry, John. 2012. Organic Chemistry (8th edition). California: Brooks/Cole, Cengage Learning
Nelson, D.L. & Cox, M.M. 2013. Lehninger Principles of Biochemistry (6th edition). New York: W. H. Freeman and Company
Petrucci, Ralph H. et al. 2011. General Chemistry: Principles and Modern Applications (10th edition). Toronto: Pearson Canada Inc.
Purba, Michael. 2007. Kimia 3B untuk SMA Kelas XII. Jakarta: Erlangga
Sudarmo, Unggul. 2007. Kimia SMA 3 untuk SMA Kelas XII. Jakarta: Phibeta
Wade, L.G. & Simek, J.W. 2016. Organic Chemistry (9th edition). Harlow: Pearson Education Limited
Artikel: Biomolekul
Kontributor: Nirwan Susianto, S.Si.
Alumni Kimia FMIPA UI
Materi StudioBelajar.com lainnya:
