Ilmu Kimia
Ilmu Kimia – Pengantar
Hampir semua hal dalam kehidupan kita melibatkan “kimia”, baik bahan kimia, reaksi kimia, energi kimia, dan lain-lain. Pada awal peradaban manusia, ketika Zaman Batu beralih ke Zaman Perunggu dan Zaman Besi, manusia tidak menyadari bahwa mereka telah melakukan reaksi kimia ketika mengubah material yang mereka temukan dan kenal sebagai ‘batu’−saat ini kita kenal sebagai mineral−menjadi berbagai logam.
Peradaban manusia selanjutnya semakin berkembang seiring dengan kemampuan untuk mentransformasi berbagai material menjadi lebih beragam dan berguna, seperti gelas, perhiasan, koin, keramik, dan lain-lain. Semua perkembangan ini tidak akan terjadi tanpa adanya kimia. Oleh karena itu, tidaklah mengherankan bila ilmu kimia disebut sebagai central science (pusat dari ilmu pegetahuan). Ilmu kimia memegang peranan yang sangat penting dalam perkembangan berbagai ilmu pengetahuan lainnya, seperti biologi, farmasi, kedokteran, pertanian, fisika, geologi, ilmu material, ilmu teknik, dan lain-lain.
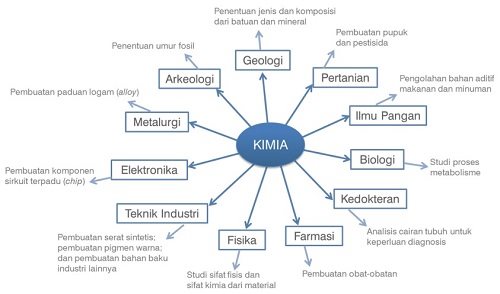
Peranan Ilmu Kimia dalam berbagai bidang
Gambaran Umum
Kimia merupakan ilmu yang mempelajari materi dan perubahan yang dialaminya. Materi adalah segala sesuattu yang menempati ruang dan memiliki massa. Semua objek yang kita lihat di sekitar kita hampir semuanya tersusun dari materi. Gas-gas yang berada di atmosfer, meskipun tidak terlihat oleh mata, juga merupakan materi−menempati ruang dan memiliki massa. Namun, cahaya matahari meskipun terlihat tidak termasuk materi karena merupakan suatu bentuk energi.
Unit penyusun terkecil dari materi adalah atom. Masing-masing unsur terdiri dari atom-atom sejenis yang khas untuk setiap unsur. Sifat dari suatu materi berkaitan dengan jenis atom-atom penyusun (komposisi) serta susunan atom-atom tersebut (struktur). Inilah yang menjadi esensi ilmu kimia, yaitu keterkaitan sifat dan perilaku atom-atom pada skala submikroskopik dengan observasi materi di sekeliling kita pada skala makroskopik.
Ruang Lingkup Kimia
Ilmu kimia mempelajari materi melingkupi susunan (komposisi), struktur, sifat, perubahan materi, serta energi yang menyertai perubahan tersebut. Berikut akan dibahas satu per satu terminologi dasar yang perlu diketahui untuk lebih memahami kimia.
1. Komposisi
Komposisi mengacu pada bagian-bagian atau komponen-komponen dari sampel sebuah materi dan perbandingan relatifnya. Air murni tersusun dari dua jenis unsur, yaitu hidrogen dan oksigen dalam perbandingan tetap tertentu. Berdasarkan massanya, komposisi air adalah 11,19% hidrogen dan 88,81% oksigen. Hidrogen peroksida, suatu senyawa yang biasa digunakan dalam antiseptik dan pemutih, juga tersusun dari hidrogen dan oksigen, namun dengan komposisi yang berbeda. Komposisi hidrogen peroksida berdasarkan massa adalah 5,93% hidrogen dan 94,07% oksigen.
2. Struktur
Struktur mengacu pada penyusunan (penataan) ruang dari partikel-partikel penyusun materi. Struktur memberikan gambaran bagaimana partikel-partikel tersebut saling terikat. Intan dan grafit, keduanya sama-sama hanya tersusun dari unsur karbon, namun keduanya memiliki struktur yang berbeda. Atom-atom karbon pada grafit tersusun dalam bentuk lapisan-lapisan. Pada intan, setiap atom karbon berikatan dengan empat atom karbon tetangganya membentuk jaringan kerangka tetrahedral.
3. Sifat
Sifat mengacu pada atribut yang dijadikan sebagai pembeda antara sampel materi yang satu dengan yang lainnya. Setiap jenis materi memiliki sifat khas yang membedakannya dari yang lain. Berdasarkan perubahan yang terjadi pada materi, sifat materi dibedakan menjadi sifat fisis dan sifat kimia. Sifat fisis dapat diamati tanpa mengubah identitas dan komposisi dari zat, misalnya warna, bau, densitas, titik leleh, titik didih, daya hantar listrik, dan kekerasan. Sifat kimia memerikan cara suatu zat berubah atau bereaksi untuk membentuk zat lain, misalnya sifat kemudahan terbakar berkaitan dengan kemampuan suatu zat terbakar dengan keberadaan oksigen.
Berdasarkan kebergantungan terhadap jumlah dari materi, sifat materi dibedakan menjadi sifat ekstensif dan sifat intensif. Sifat ekstensif bergantung pada jumlah materi, seperti massa dan volum dari suatu sampel bergantung pada jumlah zat yang ada di dalamnya. Lain halnya dengan sifat intensif yang tidak bergantung pada jumlah materi, seperti densitas, warna dan titik leleh dari suatu zat akan tetap sama, baik sampel dalam jumlah sedikit maupun sangat banyak.
4. Perubahan
Perubahan yang terjadi pada materi dibedakan menjadi perubahan fisika dan perubahan kimia. Pada perubahan fisika, sifat fisis materi berubah namun komposisi materi tidaklah berubah. Zat yang mengalami perubahan fisika tetaplah zat yang sama sebelum maupun sesudah perubahan. Contohnya, ketika air membeku, terjadi perubahan wujud dari cair menjadi padat, tetapi baik air maupun es keduanya sama terdiri dari 11,19% hidrogen dan 88,81% oksigen berdasar massa.
Semua perubahan wujud materi (dari cair ke padat, cair ke gas, padat ke gas, dan sebaliknya) termasuk perubahan fisika. Pada perubahan kimia (reaksi kimia), satu atau lebih jenis materi berubah menjadi jenis materi yang baru dengan komposisi yang berbeda dengan semula. Contohnya, ketika gas hidrogen dibakar di udara, terjadi kombinasi antara hidrogen dan oksigen yang berada di udara membentuk air.
Cabang-cabang Ilmu Kimia
Ilmu kimia dibagi menjadi lima cabang utama, antara lain:
- Kimia analitik mempelajari identifikasi zat-zat apa yang ada (analisis kualitatif) serta deteksi berapa jumlah masing-masing zat (analisis kuantitatif) dalam suatu sampel materi.
- Kimia fisik menerapkan teori matematika dan metode fisika pada sifat materi untuk mempelajari proses kimia dan perubahan energi yang terlibat.
- Kimia organik mempelajari struktur, sifat, dan reaksi dari senyawa-senyawa organik. Senyawa organik secara umum adalah senyawa yang memiliki ikatan antara karbon-hidrogen.
- Kimia anorganik mempelajari segala zat yang tidak termasuk senyawa organik. Senyawa-senyawa karbon sederhana seperti karbon monoksida, karbon dioksida, dan senyawaan karbonat tergolong sebagai senyawa anorganik.
- Biokimia mempelajari proses-proses kimia yang ada dalam makhluk hidup.
Besaran Pokok dan Besaran Turunan
Percakapan Bahasa Inggris
Keanekaragaman Hayati
Metode Ilmiah
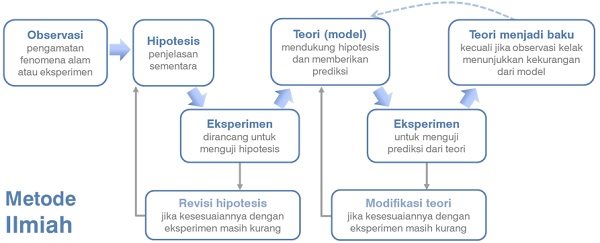
Kimia, sebagai bagian dari sains, dikembangkan oleh para ilmuwan dari sejak dahulu kala dengan menggunakan suatu pendekatan sistematis dalam mengolah dan memahami informasi-informasi relevan yang didapat dari berbagai eksperimen. Prosedur pendekatan sistematis dalam memperoleh ilmu pengetahuan ini dikenal sebagai metode ilmiah. Tahap-tahap dalam metode ilmiah dapat dilihat dalam skema berikut:
Contoh Soal dan Pembahasan tentang Ilmu Kimia
Contoh Soal 1
Berikut adalah beberapa peristiwa perubahan materi di sekitar kita.
- kamper menyublim
- fotosintesis
- besi berkarat
- menyolder
- lilin terbakar
- kayu melapuk
Peristiwa yang termasuk perubahan kimia adalah …
A. 1, 2, 4, 5
B. 2, 3, 4, 5
C. 2, 3, 4, 6
D. 2, 3, 5, 6
E. 3, 4, 5, 6
Jawab: D
Perubahan kimia ditandai dengan terbentuknya zat baru. Fotosintesis merupakan reaksi kimia di mana karbon dioksida dan air diubah menjadi glukosa dan oksigen. Besi berkarat merupakan besi yang teroksidasi menjadi oksida besi. Lilin terbakar merupakan reaksi pembakaran yang dapat menghasilkan karbon dioksida dan uap air. Kayu melapuk merupakan reaksi penguraian matriks polisakarida kayu menjadi senyawa-senyawa yang lebih sederhana.
Contoh Soal 2
Berikut adalah langkah-langkah dalam metode ilmiah.
- menarik kesimpulan
- mempublikasikan hasil
- menganalisis data
- mengusulkan hipotesis
- merumuskan masalah
- melakukan eksperimen
Urutan langkah metode ilmiah yang benar adalah …
- 6−5−4−3−2−1
- 5−4−6−3−1−2
- 4−6−5−3−2−1
- 3−4−5−6−1−2
- 4−5−3−6−1−2
Jawab: B
Urutan langkah dalam metode ilmiah, yaitu: merumuskan masalah → mengusulkan hipotesis → melakukan eksperimen → menganalisis data → menarik kesimpulan → mempublikasikan hasil.
Referensi
Atkins, Peter & Jones, Loretta. 2010. Chemical Principles: The Quest for Insight (5th edition). New York: W.H. Freeman & Company
Brown, Theodore L. et al. 2017. Chemistry: The Central Science (14th edition). New Jersey: Pearson Education, Inc.
Johari, J.M.C. & Rachmawati, M. 2009. Kimia SMA dan MA untuk Kelas X Jilid 1. Jakarta: Esis
Petrucci, Ralph H. et al. 2017. General Chemistry: Principles and Modern Applications (11th edition). Toronto: Pearson Canada Inc.
Whitten, Kenneth. W. et al. 2014. Chemistry (10th edition). California: Brooks/Cole Cengage Learning
Kontributor: Nirwan Susianto, S.Si.
Alumni Kimia FMIPA UI
Materi Kimia lainnya di StudioBelajar.com:
